原子の英語表現
本項では以下の内容を解説しています。
- ・原子に関連する英語表現
- ・関連する用語の一覧
【1】原子の英語表現
物質を構成する最小単位である原子は英語で"atom"といいます。
原子は陽子(proton)と中性子(neutron)から構成される原子核(atomic nucleus)と、原子核の周囲に分布する電子(electron)から構成されます。
下図に原子を構成する陽子・中性子・電子の概略図を示します。
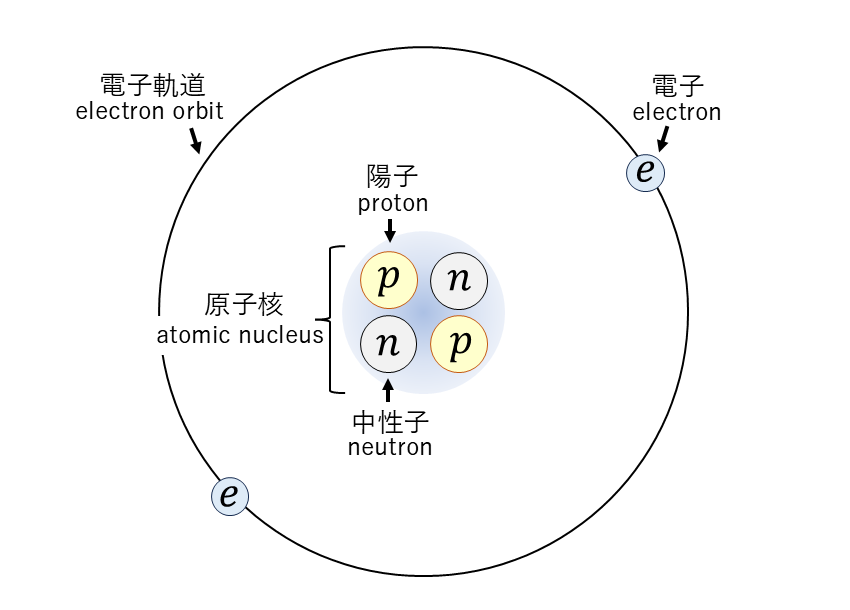
原子核は正の電荷を持つ陽子と電荷を持たない中性子から構成されており、正の電荷を帯びています。
一方、電子は負の電荷を持ちます。そのため、正の電荷の原子核と負の電荷の電子の間にクーロン力(coulomb force)が働きます。
・関連する例文
『原子は陽子と中性子からなる原子核と、その周りを回る電子から構成されています。』は英語で以下のように表します。
"An atom consists of a nucleus of protons and neutrons surrounded by moving electrons."
『水素原子の原子核には、1つの陽子があります』は英語で以下のように表します。
"A hydrogen nucleus has one proton."
『陽子は正の電荷を持ちます』は英語で以下のように表します。
"Protons have a positive charge."
電荷の正負を言い表すときは 正の電荷を"positive charge"、負の電荷を"negative charge"といいます。
【2】電子の英語表現
原子や分子の電子が存在する軌道を電子軌道といいます。電子軌道は英語では "electron orbital" もしくは "orbital" といいます。
また、1つの原子の電子軌道について述べるときは原子軌道(atomic orbital)、分子の電子軌道について述べるときは分子軌道(molecular orbital)ともいいます。
【2-1】電子軌道の英語表現
原子核の周囲に存在する電子の配置は、原子核を中心に電子殻(electron shell)という層をなしていると考えます。
電子殻は原子核に近い方から順に、K殻、L殻、M殻、N殻…と名前が付けられています。
英語では、K shell、L shell、M shell、N shell…といいます。
下図に電子殻の概略図を示します。
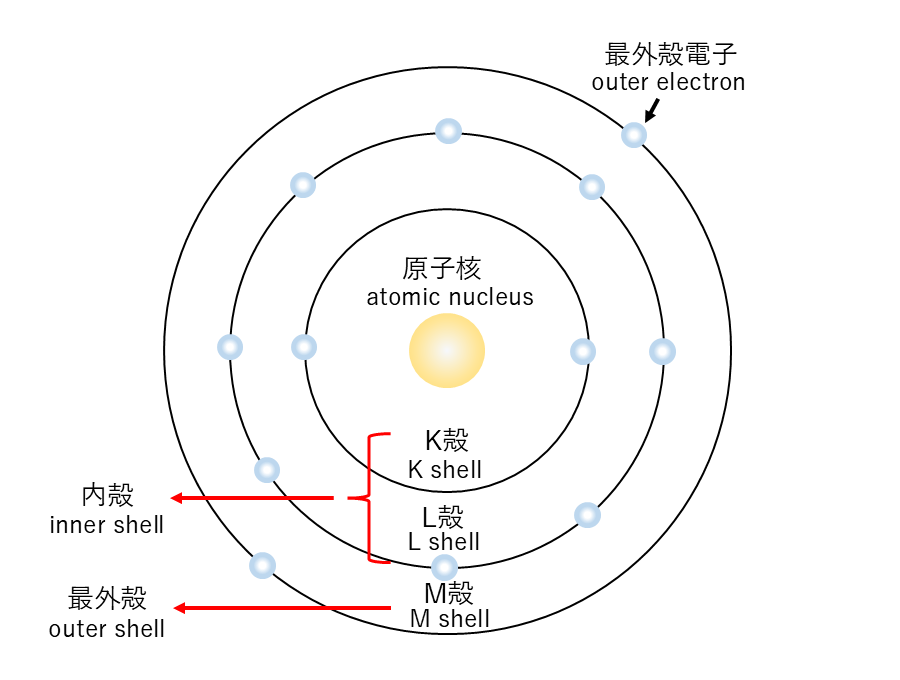
電子殻の最も外側に位置する電子殻を最外殻(outer shell)、最外殻にある電子を最外殻電子(outer electron)といいます。
特に、原子間の化学結合に関わる電子を価電子(valence electron)といいます。
最も外側にある電子殻のすべての軌道に電子が満たされていない場合、最外殻電子のことを価電子ともいいます。
一方、最も外側に位置する電子殻のすべての軌道に電子が満たされている場合を閉殻(closed shell)といいます。
原子が閉殻である場合は、化学的に安定となり他の原子と反応しにくい状態となります。
・関連する例文
『原子の一番目の電子殻は最大2つまで電子が入ることができます。』は英語で以下のように表します。
"The first electron shell of an atom can hold up to two electrons."
"hold up to A" は『最大Aまで保持する』ことを意味します。電子殻に対して使用すれば『最大A個まで(電子を)収容する』ことを表します。
『ヘリウムはK殻に2つの電子を持っています。』は英語で以下のように表します。
"Helium has two electrons in its K shell."
『原子核から\(\large{\hspace{1pt}n\hspace{2pt}}\)番目の電子殻には\(\large{\hspace{1pt}2n^2\hspace{2pt}}\)個の電子が収容できます。』は英語で以下のように表します。
"The n-th electron shell from the atomic nucleus can hold up to 2 n squared electrons."
\(\large{\hspace{1pt}X^2\hspace{2pt}}\)を英語では "X squared" もしくは "the square of X" といいます。(数学のべき乗を表す英語に関してはべき乗の英語表現で解説しています。)
【2-2】量子数の英語表現
原子の電子軌道は量子数(quantum number)により決定されます。
原子に関係する量子数には、主量子数(principal quantum number)、方位量子数(azimuthal quantum number)、磁気量子数(magnetic quantum number)の3種類があります。
\(\large{3\hspace{2pt}}\)つの量子数によって決定される各電子軌道には、異なるスピンをもつ\(\large{\hspace{1pt}2\hspace{2pt}}\)つの電子が存在することができます。
このスピンを表す量子数をスピン量子数(spin quantum number)といいます。
量子数の記号と名称、英語の読み方をまとめると以下のようになります。
| 記号 | 名称 | 英語 |
|---|---|---|
| n | 主量子数 | principal quantum number |
| l | 方位量子数 | azimuthal quantum number |
| m | 磁気量子数 | magnetic quantum number |
| s | スピン量子数 | spin quantum number |
・関連する例文
『主量子数は電子のエネルギー準位の大きさを表します。』は英語で以下のように表します。
"The principal quantum number represents the energy level of an electron."
『主量子数は任意の正の整数の値をとります。』は英語で以下のように表します。
"The principal quantum number can have any positive integar value."
『方位量子数は\(\large{\hspace{1pt}0\hspace{2pt}}\)から\(\large{\hspace{1pt}n-1\hspace{2pt}}\)までの値をとります。』は英語で以下のように表します。
"The azimuthal quantum number can have any value from 0 to n minus 1."
『スピン量子数は\(\displaystyle\large{\hspace{1pt}\frac{1}{2}\hspace{2pt}}\)もしくは\(\displaystyle\large{\hspace{1pt}-\frac{1}{2}\hspace{2pt}}\)の値をとります。』は英語で以下のように表します。
"The spin quantum number can be eihter one-half or negative one-half."
分数の\(\displaystyle\large{\hspace{1pt}\frac{1}{2}\hspace{2pt}}\)は one-half もしくは a half という表現を使用します。
(分数の英語については分数の英語表現で解説しています。)
・例文の補足 | minus と negative の使い分け
方位量子数の例文では『\(\large{\hspace{1pt}n-1\hspace{2pt}}\)』を n minus 1 と解説しました。
一方、スピン量子数の例文では『\(\displaystyle\large{\hspace{1pt}-\frac{1}{2}\hspace{2pt}}\)』を negative one-half としました。
同じ見た目の『\(\large{\hspace{1pt}-\hspace{2pt}}\)』でも引き算を表すのか、負の符号を表すのかで使い分けをします。
『\(\large{\hspace{1pt}n-1\hspace{2pt}}\)』のように引き算の演算を表す場合は minus、負の符号を表す場合は negative を使用します。
【3】原子の英語表現に関連する単語
原子の英語表現に関連する単語を一覧にまとめます。
・原子の構造に関連する英単語
以下に、原子の構造を表す英単語を示します。
| 用語 | 意味 |
|---|---|
| ・atom | ・原子 |
| ・proton | ・陽子 |
| ・neutron | ・中性子 |
| ・electron | ・電子 |
| ・atomic nucleus | ・原子核 |
| ・quark | ・クォーク |
| ・fermion | ・フェルミ粒子 |
| ・boson | ・ボース粒子 |
・電子殻に関連する英単語
以下に、電子殻を表す英単語を示します。
| 用語 | 意味 |
|---|---|
| ・(electron) orbital | ・電子軌道 |
| ・atomic orbital | ・原子軌道 |
| ・molecular orbital | ・分子軌道 |
| ・electron shell | ・電子殻 |
| ・inner shell | ・内殻 |
| ・outer shell | ・外殻 |
| ・outer electron | ・最外殻電子 |
| ・valence electron | ・荷電子 |
| ・closed shell | ・閉殻 |
| ・noble gas | ・貴ガス/希ガス(閉殻であり化学的に安定した元素) |
| ・electron cloud | ・電子雲 |
・量子数に関連する英単語
以下に、量子数に関連する英単語を示します。
| 用語 | 意味 |
|---|---|
| ・principal quantum number | ・主量子数 |
| ・azimuthal quantum number | ・方位量子数 |
| ・magnetic quantum number | ・磁気量子数 |
| ・spin quantum number | ・スピン量子数 |
| ・energy level | ・エネルギー順位 |
| ・pauli exclusion principle | ・パウリの排他原理(1つの原子軌道に1つの電子しか収容できないことを説明する原理) |
| ・electronic configuration | ・電子配置 |
・原子の状態に関連する英単語
以下に、原子の状態を表す英単語を示します。
| 用語 | 意味 |
|---|---|
| ・atomic number | ・原子番号(陽子の数) |
| ・atomic mass | ・原子量 |
| ・ion | ・イオン(電子を失ったり、電子を余剰に持ち電荷を持った原子) |
| ・positive ion | ・陽イオン(正の電荷を帯びた原子) |
| ・negative ion | ・陰イオン(負の電荷を帯びた原子) |
| ・isotope | ・同位体(中性子の数の異なる原子) |
| ・molecule | ・分子(複数の原子が結合した粒子) |
| ・compound | ・化合物(異なる種類の元素が結合してできた物質) |